Physiologie digestive
Définitions et généralités :
La digestion est la fonction qui permet de dégrader les aliments d’origine animale ou végétale en éléments simples qui seront, après absorption digestive, utilisés soit pour leur pouvoir énergétique, soit comme éléments de base de construction plastique.
 La dégradation des aliments se fait par des moyens mécaniques et par des enzymes sécrétées tout au long du tube digestif.
La dégradation des aliments se fait par des moyens mécaniques et par des enzymes sécrétées tout au long du tube digestif.
Le terme « digestion » désigne habituellement différentes fonctions :
1. Fonction motrice, par laquelle les aliments subissent des transformations mécaniques qui les homogénéisent et les mêlent aux sécrétions digestives
2. Fonction sécrétoire : par sécrétion on désigne le transport d’eau,d’électrolyse, de substances depuis les cellules du tractus digestif vers la lumière digestive ou le sang
3. Fonction d’absorption : on désigne par absorption le passage des éléments simples de la lumière digestive vers le milieu intérieur. Donc, si un aliment est constitué de molécules simples (glucose), il est absorbé sans avoir à subir la digestion.
4. Fonction excrétrice : l’excrétion concerne uniquement les produits qui vont être éliminés.
Mastication :
Définition
L’ensemble des mouvements volontaires de la mâchoire, de la langue, et des joues qui entraîne la dilacération des aliments.
Les aliments sont broyés et ramollis.
Les aliments sont mêlés à la salive ce qui augmente l’hydratation du bol alimentaire et le contact avec les enzymes salivaires (amylase salivaire).
Les actions enzymatiques ultérieures sont accrues par ce temps buccal qui augmente la surface attaquable des aliments.
Contrôle de la mastication
Phénomène volontaire chez l’homme adulte.
Contrôle supérieur cortical dont le centre moteur est situé au niveau de la base du cortex moteur prérolantique.
La réalisation pratique est contrôlée par un ensemble de réflexes dont les centres sont situés au niveau protubérantiel.
Ces réflexes s’observent chez les enfants mais perdent leur importance lors du développement ultérieur de l’homme. Ils peuvent être retrouvés lors de l’examen clinique chez le patient comateux (atteinte du tronc cérébral).
Salivation :
Généralités :
Le volume quotidien de salive produite est compris entre 1000 et 1500 ml.
La sécrétion digestive est très limitée en période inter – digestive et pendant la nuit.
La sécrétion s’accroît 4 à 8 fois pendant lors de l’alimentation.
L’essentiel provient surtout des glandes parotides (~2/3) et sous maxillaires (~1/3).
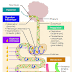
La salive est produite par 3 paires de glandes :
• Les parotides situées en avant et en dessous des oreilles.
• Les glandes sublinguales situées dans la partie antérieure du plancher buccal.
• Les glandes sous-maxillaires situées sous la mâchoire.
Ces glandes sont formées en bouquets d’acini reliés au canal excréteur : le canal de Sténon pur la parotide (face interne des joues), le canal de Wharton pour les glandes sous-maxillaires (plancher de la bouche des deux côtés de la langue).
Les cellules acineuses sont responsables de la sécrétion de la salive primaire
• Cellules zymogènes (séreuses) : spécialisées dans la synthèse et la sécrétion hydro électrolytiques.
• Cellules à mucus synthétisent les mucines.
Le rôle de la salive :
Le rôle de la salive en physiologie humaine
• Effet lubrifiant sur le bol alimentaire.
• Digestion de l’amidon (l’amylase salivaire).
• Hydratation du bol alimentaire.
• Solubilisation des substances qui vont donner le goût à l’alimentation.
• Rinçage de la bouche et effets antiseptiques.
Composition hydro-électrolytiques:
La salive est constituée à 95% d’eau. Les concentrations d’électrolytes varient en fonction du débit salivaire et de l’état d’hydratation de l’organisme.
1. La salive primaire
La composition ionique de la salive primaire est proche de celle du plasma. En fonction de leur sécrétion ionique, on distingue :
Les glandes salivaires sécrétant un liquide riche en chlore (Cl-)
Les glandes salivaires sécrétant un liquide riche en bicarbonates (HCO3-)
Dans les 2 cas, la composition en sodium (Na+) est proche de celle du plasma etce celle du potassium (K+) hypertonique (10-15mM).
2. La salive définitive
Elle est élaborée dans les canaux excréteurs où il se produit
Réabsorption active de sodium (Na+) et de chlore (Cl-)
Sécrétion active de bicarbonates (HCO3-) et de potassium (K+)
Les canaux excréteurs sont peu perméables à l’eau et les échanges ioniques (réabsorption active Na+) aboutissent à la formation d’un liquide hypotonique par rapport au plasma (30 à 300m/Osm/L selon le débit de sécrétion).
Composition organique de la salive :
Les composants organiques de la salive sont essentiellement des protéines synthétisées dans les cellules acineuses et sécrétées par des mécanismes d’exocytose.
• Les enzymes salivaires :
L’amylase salivaire est une glycoprotéine de 55kDa. Elle attaque les liaisons alpha 1-4 glucosidiques de l’amidon à pH neutre (optimal 6,5 à 7) libérant ainsi du maltose et des oligomères glucosidiques (dextrines). Son action est inhibée par l’acidité gastrique.
Le lysozyme : petite protéine glycolytique (rôle antiseptique)
• Les mucines salivaires :
Grosses molécules (>106 kDa) qui donnent à la salive sa viscosité. Elles sont constituées de chaînes polypeptidiques sur les quelles se greffent des chaînes glucidiques.
Deux familles moléculaire différentes : les glycoprotéines (ramifications glucidiques courtes) et les mucopolysaccharides acides (ramifications très longes formées de l’association sucre-acide uronique).
• Les immunoglobulines
A côté des immunoglobulines plasmatiques qui passent dans la salive par diffusion (IgA, Ig G et IgM) celle-ci contient également des Ig A sécrétoires.
Les Ig A sécrétoires ont un rôle fondamental dans les défenses antibactériennes au niveau du tube digestif.
 La déglutition :
La déglutition :
Anatomie de l'oesophage
Sphincter supérieur SSO : constitue la partie supérieure de l’oesophage. Le muscle strié crico-pharyngé y détermine une zone de haute pression.
Corps de l’oesophage : tiers supérieur (muscle strié) – deux tiers inférieur (fibres musculaires lisses)
Sphincter inférieur SSI : constitué de fibres musculaires lisses correspond à une zone de haute pression.
La déglutition est l’ensemble des mouvements qui font passer le bol alimentaire,de bouche à l’estomac.
On décrit 3 temps à la déglutition : temps buccal, temps pharyngien,oesophagien.
Temps buccal : phase volontaire, bouche fermée, pointe de la langue en contact avec la partie antérieure du palais. En un mouvement AV vers AR la base de la langue s’élève et fait basculer le bol dans le pharynx.
Temps pharyngien : très court, arrêt de la ventilation (apnée), fermeture de l’orifice postérieur des fosses nasales par élévation du voile du palais. Le larynx bascule en HT et en AV. L’épiglotte se rabat en auvent et les cordes
vocales se ferment.
Temps oesophagien : le bol alimentaire déclenche un mouvement péristaltique, contraction circulaire sur 4-8 cm de long très efficace (déglutition tête en l’air) d’une durée de 2 à 4 secondes).
Deux secondes après la déglutition, le relâchement du SSI entraîne une chute de pression de repos du SSI qui persiste jusqu’à ce que l’onde péristaltique atteigne la jonction oeso-gastrique.
Physiologie Gastrique:
Structure de l'estomac
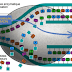
L’estomac est une poche en forme de « J » constitué de 3 parties :
Grosse tubérosité : (fundus), partie supérieure qui correspond à la poche d’air.
Corps : partie moyenne, épaisse
Antre et région pylorique, fibres musculaires lisses très développées
Musculature de l'estomac
Comporte 3 couches de fibres musculaires lisses, externe longitudinale,interne circulaire, et couche moyenne oblique qui limite la distension de l’estomac dans le plan vertical.
Au niveau du pylore, un épaississement des fibres constitue un sphincter anatomique.
Innervation de l'estomac
La musculeuse de l’estomac est innervée par un système nerveux intrinsèque qui comprenant les plexus d’Auerhbach et de Meissner.
Les branches du pneumogastrique (X) constituent l’innervation extrinsèque parasympathique dont l’effet est d’accroître la mobilité et le tonus.
Les fibres sympathiques du plexus coeliaque sont inhibitrices de la motilité.
Phénomènes électro-mécanique:
L’activité motrice de l’estomac
Les activités motrice de l’estomac visent à assurer le brassage des aliments et l’évacuation progressive vers le duodénum.
Les cellules musculaires possèdent des propriétés électrophysiologies différentes selon les régions de l’estomac.
Les cellules musculaires de la partie proximale de l’estomac ont un potentiel de repos faible (-48mV) et élevé dans les cellules distales (-70mV).
Mise en jeu humorale
Le contact des peptiques, acides aminés (récepteur au L-tryptophane), de sucres et surtout de graisses avec la muqueuse duodénale provoque la libération dans la circulation d’entérogastrones qui inhibent l’évacuation de l’estomac. On a invoqué de nombreux agents : gastrine, sécrétine, cholécystokinine (CCK).
Leur action est cependant complexe et non totalement élucidée.
La gastrine ralentie l’évacuation bien qu’elle augmente l’activité électrique et la force des contractions gastriques.
La CCK sécrétée par la muqueuse jéjunale en réponse au contact des graisses du chyme, agit comme un inhibiteur compétitif qui bloque les effets de la gastrine sur la motilité de l’estomac.
La sécrétine sécrétée par la muqueuse duodénale au contact de l’acidité du chyme, diminue la motilité gastrique.
La GIP (gastric inhibitory peptide) secrétée par l’intestin grêle en réponse au contact des graisses du chyme diminue la motilité gastrique.
Glandes exocrines de la muqueuse gastrique
La muqueuse gastrique contient de très nombreuses glandes exocrines (100 orifices/mm2)
Cellules principales : pepsinogène forme inactive de la pepsine.
Cellules bordantes ou pariétales : sécrète de l’acide chlorhydrique
Cellules à mucus : sécrète du mucus essentiellement au niveau du collet des glandes
Selon la prédominance des différents types cellulaires, on distingue 3 zones :
Zone péricardiale : cellules à mucus uniquement
Corps : 3 types cellulaires (principales, pariétales et à mucus)
Zone antro-pylorique : cellules principales et à mucus.
Glandes endocrines de la muqueuse gastrique
A l’opposé des cellules exocrines qui élaborent la sécrétion externe de l’estomac, les cellules des glandes endocrines déversent leurs produits dans le sang.
Cellules sécrétant la gastrine (cellules G), cellules de forme triangulaire, surtout présentes dans l’antre gastrique.
Cellules à somatostatine (cellule D), ubiquitaire de l’estomac.
Cellules à sérotonine (entérochromaffines), surtout présentes dans le fundus et l’antre gastrique
Rôle de la sécrétion acide (HCL) gastrique
La digestion est la fonction qui permet de dégrader les aliments d’origine animale ou végétale en éléments simples qui seront, après absorption digestive, utilisés soit pour leur pouvoir énergétique, soit comme éléments de base de construction plastique.
 La dégradation des aliments se fait par des moyens mécaniques et par des enzymes sécrétées tout au long du tube digestif.
La dégradation des aliments se fait par des moyens mécaniques et par des enzymes sécrétées tout au long du tube digestif.Le terme « digestion » désigne habituellement différentes fonctions :
1. Fonction motrice, par laquelle les aliments subissent des transformations mécaniques qui les homogénéisent et les mêlent aux sécrétions digestives
2. Fonction sécrétoire : par sécrétion on désigne le transport d’eau,d’électrolyse, de substances depuis les cellules du tractus digestif vers la lumière digestive ou le sang
3. Fonction d’absorption : on désigne par absorption le passage des éléments simples de la lumière digestive vers le milieu intérieur. Donc, si un aliment est constitué de molécules simples (glucose), il est absorbé sans avoir à subir la digestion.
4. Fonction excrétrice : l’excrétion concerne uniquement les produits qui vont être éliminés.
Mastication :
Définition
L’ensemble des mouvements volontaires de la mâchoire, de la langue, et des joues qui entraîne la dilacération des aliments.
Les aliments sont broyés et ramollis.
Les aliments sont mêlés à la salive ce qui augmente l’hydratation du bol alimentaire et le contact avec les enzymes salivaires (amylase salivaire).
Les actions enzymatiques ultérieures sont accrues par ce temps buccal qui augmente la surface attaquable des aliments.
Contrôle de la mastication
Phénomène volontaire chez l’homme adulte.
Contrôle supérieur cortical dont le centre moteur est situé au niveau de la base du cortex moteur prérolantique.
La réalisation pratique est contrôlée par un ensemble de réflexes dont les centres sont situés au niveau protubérantiel.
Ces réflexes s’observent chez les enfants mais perdent leur importance lors du développement ultérieur de l’homme. Ils peuvent être retrouvés lors de l’examen clinique chez le patient comateux (atteinte du tronc cérébral).
Salivation :
Généralités :
Le volume quotidien de salive produite est compris entre 1000 et 1500 ml.
La sécrétion digestive est très limitée en période inter – digestive et pendant la nuit.
La sécrétion s’accroît 4 à 8 fois pendant lors de l’alimentation.
L’essentiel provient surtout des glandes parotides (~2/3) et sous maxillaires (~1/3).
La salive est produite par 3 paires de glandes :
• Les parotides situées en avant et en dessous des oreilles.
• Les glandes sublinguales situées dans la partie antérieure du plancher buccal.
• Les glandes sous-maxillaires situées sous la mâchoire.
Ces glandes sont formées en bouquets d’acini reliés au canal excréteur : le canal de Sténon pur la parotide (face interne des joues), le canal de Wharton pour les glandes sous-maxillaires (plancher de la bouche des deux côtés de la langue).
Les cellules acineuses sont responsables de la sécrétion de la salive primaire
• Cellules zymogènes (séreuses) : spécialisées dans la synthèse et la sécrétion hydro électrolytiques.
• Cellules à mucus synthétisent les mucines.
Le rôle de la salive :
Le rôle de la salive en physiologie humaine
• Effet lubrifiant sur le bol alimentaire.
• Digestion de l’amidon (l’amylase salivaire).
• Hydratation du bol alimentaire.
• Solubilisation des substances qui vont donner le goût à l’alimentation.
• Rinçage de la bouche et effets antiseptiques.
Composition hydro-électrolytiques:
La salive est constituée à 95% d’eau. Les concentrations d’électrolytes varient en fonction du débit salivaire et de l’état d’hydratation de l’organisme.
1. La salive primaire
La composition ionique de la salive primaire est proche de celle du plasma. En fonction de leur sécrétion ionique, on distingue :
Les glandes salivaires sécrétant un liquide riche en chlore (Cl-)
Les glandes salivaires sécrétant un liquide riche en bicarbonates (HCO3-)
Dans les 2 cas, la composition en sodium (Na+) est proche de celle du plasma etce celle du potassium (K+) hypertonique (10-15mM).
2. La salive définitive
Elle est élaborée dans les canaux excréteurs où il se produit
Réabsorption active de sodium (Na+) et de chlore (Cl-)
Sécrétion active de bicarbonates (HCO3-) et de potassium (K+)
Les canaux excréteurs sont peu perméables à l’eau et les échanges ioniques (réabsorption active Na+) aboutissent à la formation d’un liquide hypotonique par rapport au plasma (30 à 300m/Osm/L selon le débit de sécrétion).
Composition organique de la salive :
Les composants organiques de la salive sont essentiellement des protéines synthétisées dans les cellules acineuses et sécrétées par des mécanismes d’exocytose.
• Les enzymes salivaires :
L’amylase salivaire est une glycoprotéine de 55kDa. Elle attaque les liaisons alpha 1-4 glucosidiques de l’amidon à pH neutre (optimal 6,5 à 7) libérant ainsi du maltose et des oligomères glucosidiques (dextrines). Son action est inhibée par l’acidité gastrique.
Le lysozyme : petite protéine glycolytique (rôle antiseptique)
• Les mucines salivaires :
Grosses molécules (>106 kDa) qui donnent à la salive sa viscosité. Elles sont constituées de chaînes polypeptidiques sur les quelles se greffent des chaînes glucidiques.
Deux familles moléculaire différentes : les glycoprotéines (ramifications glucidiques courtes) et les mucopolysaccharides acides (ramifications très longes formées de l’association sucre-acide uronique).
• Les immunoglobulines
A côté des immunoglobulines plasmatiques qui passent dans la salive par diffusion (IgA, Ig G et IgM) celle-ci contient également des Ig A sécrétoires.
Les Ig A sécrétoires ont un rôle fondamental dans les défenses antibactériennes au niveau du tube digestif.
 La déglutition :
La déglutition :Anatomie de l'oesophage
Sphincter supérieur SSO : constitue la partie supérieure de l’oesophage. Le muscle strié crico-pharyngé y détermine une zone de haute pression.
Corps de l’oesophage : tiers supérieur (muscle strié) – deux tiers inférieur (fibres musculaires lisses)
Sphincter inférieur SSI : constitué de fibres musculaires lisses correspond à une zone de haute pression.
La déglutition est l’ensemble des mouvements qui font passer le bol alimentaire,de bouche à l’estomac.
On décrit 3 temps à la déglutition : temps buccal, temps pharyngien,oesophagien.
Temps buccal : phase volontaire, bouche fermée, pointe de la langue en contact avec la partie antérieure du palais. En un mouvement AV vers AR la base de la langue s’élève et fait basculer le bol dans le pharynx.
Temps pharyngien : très court, arrêt de la ventilation (apnée), fermeture de l’orifice postérieur des fosses nasales par élévation du voile du palais. Le larynx bascule en HT et en AV. L’épiglotte se rabat en auvent et les cordes
vocales se ferment.
Temps oesophagien : le bol alimentaire déclenche un mouvement péristaltique, contraction circulaire sur 4-8 cm de long très efficace (déglutition tête en l’air) d’une durée de 2 à 4 secondes).
Deux secondes après la déglutition, le relâchement du SSI entraîne une chute de pression de repos du SSI qui persiste jusqu’à ce que l’onde péristaltique atteigne la jonction oeso-gastrique.
Physiologie Gastrique:
Structure de l'estomac
L’estomac est une poche en forme de « J » constitué de 3 parties :
Grosse tubérosité : (fundus), partie supérieure qui correspond à la poche d’air.
Corps : partie moyenne, épaisse
Antre et région pylorique, fibres musculaires lisses très développées
Musculature de l'estomac
Comporte 3 couches de fibres musculaires lisses, externe longitudinale,interne circulaire, et couche moyenne oblique qui limite la distension de l’estomac dans le plan vertical.
Au niveau du pylore, un épaississement des fibres constitue un sphincter anatomique.
Innervation de l'estomac
La musculeuse de l’estomac est innervée par un système nerveux intrinsèque qui comprenant les plexus d’Auerhbach et de Meissner.
Les branches du pneumogastrique (X) constituent l’innervation extrinsèque parasympathique dont l’effet est d’accroître la mobilité et le tonus.
Les fibres sympathiques du plexus coeliaque sont inhibitrices de la motilité.
Phénomènes électro-mécanique:
L’activité motrice de l’estomac
Les activités motrice de l’estomac visent à assurer le brassage des aliments et l’évacuation progressive vers le duodénum.
Les cellules musculaires possèdent des propriétés électrophysiologies différentes selon les régions de l’estomac.
Les cellules musculaires de la partie proximale de l’estomac ont un potentiel de repos faible (-48mV) et élevé dans les cellules distales (-70mV).
Mise en jeu humorale
Le contact des peptiques, acides aminés (récepteur au L-tryptophane), de sucres et surtout de graisses avec la muqueuse duodénale provoque la libération dans la circulation d’entérogastrones qui inhibent l’évacuation de l’estomac. On a invoqué de nombreux agents : gastrine, sécrétine, cholécystokinine (CCK).
Leur action est cependant complexe et non totalement élucidée.
La gastrine ralentie l’évacuation bien qu’elle augmente l’activité électrique et la force des contractions gastriques.
La CCK sécrétée par la muqueuse jéjunale en réponse au contact des graisses du chyme, agit comme un inhibiteur compétitif qui bloque les effets de la gastrine sur la motilité de l’estomac.
La sécrétine sécrétée par la muqueuse duodénale au contact de l’acidité du chyme, diminue la motilité gastrique.
La GIP (gastric inhibitory peptide) secrétée par l’intestin grêle en réponse au contact des graisses du chyme diminue la motilité gastrique.
Glandes exocrines de la muqueuse gastrique
La muqueuse gastrique contient de très nombreuses glandes exocrines (100 orifices/mm2)
Cellules principales : pepsinogène forme inactive de la pepsine.
Cellules bordantes ou pariétales : sécrète de l’acide chlorhydrique
Cellules à mucus : sécrète du mucus essentiellement au niveau du collet des glandes
Selon la prédominance des différents types cellulaires, on distingue 3 zones :
Zone péricardiale : cellules à mucus uniquement
Corps : 3 types cellulaires (principales, pariétales et à mucus)
Zone antro-pylorique : cellules principales et à mucus.
Glandes endocrines de la muqueuse gastrique
A l’opposé des cellules exocrines qui élaborent la sécrétion externe de l’estomac, les cellules des glandes endocrines déversent leurs produits dans le sang.
Cellules sécrétant la gastrine (cellules G), cellules de forme triangulaire, surtout présentes dans l’antre gastrique.
Cellules à somatostatine (cellule D), ubiquitaire de l’estomac.
Cellules à sérotonine (entérochromaffines), surtout présentes dans le fundus et l’antre gastrique
Rôle de la sécrétion acide (HCL) gastrique
- Stérilise le contenu gastrique
- Transforme le pepsinogène en pepsine
- Débute l’inversion du saccharose
- Transforme le fer ferreux en fer ferrique
- Ionise le calcium (absorption facilitée)
Généralités
- L’intestin est le siège principal de l’absorption des nutriments
- L’absorption est la résultante de flux permanents et abondants d’eau et de substances dissoutes de la lumière vers le milieu extracellulaire et vice-versa
- Le débit liquidien duodénal est de 10 L/jour avec une absorption nette de 9L/jour dans l’intestin grêle (1L/jour atteint le colon).
Anatomie fonctionnelle :
Duodénum : 30 cm de long, du pylore à l’angle de Treitz mélange avec les sécrétions pancréatique et biliaire
absorption passive par équilibration osmotique, rapide et peu régulée et intéresse surtout les glucides, l’eau et électrolytes.
Jéjunum : 3 à 4 m de long,absorption des glucides,des lipides et des protides,lieu de mouvements hydro-électrolytiques.
Iléon : 1 m de long ,absorption spécifique vit B12, sels biliaires.
Digestion et absorption des hydrates de carbones
Les glucides alimentaires : amidons et cellulose.
Les processus de digestion (hydrolyse) et d’absorption sont indissociables. La digestion des sucres débute dans la lumière intestinale sous l’action des alpha amylases salivaires et pancréatiques qui clivent les amidons en oligosaccharides et disaccharides. La cellulose est résistante aux amylases. Les dimères et oligosaccharides diffusent à travers le glycocalix
Action des disaccharidases de la bordure en brosse des entérocytes : (saccharase isomaltose +++) : hydrolyse en glucose et fructose.
Absorption et diffusion passive intercellulaire et intracellulaire.
La régulation fine de l’absorption des glucides se fait grâce à des protéines de transport dans la membrane plasmique.
Absorption des protéines
Origine
Exogène : 70 à 100 g par jour
Endogène : enzymes et glycoprotéines salivaires gastriques, pancréatiques et intestinaux (35g/j) et biliaires (10g/j).
Digestion intraluminale
Digestion incomplète par l’action des enzymes gastriques (pepsine) et pancréatiques (trypsine, chymotrypsine, peptidases) : production d’acides aminés et des peptides de taille variables.
Digestion entérocytaire
Au niveau de la bordure en brosse de l’entérocytes des peptidases.Clive en acides aminés et di-tri-peptides absorbés à travers la membrane.
Absorption intestinale des acides aminés
Au niveau de l’intestin proximal
Système de transport actif secondaire (gradient électrochimique de Na+)
Système de transport : diffusion facilitée.
Absorption intestinale des peptides
Pour les di et tripeptides : système spécifique co transport H+ - peptide
Le gradient H+ dépend de l’activité Na – K ATPase.
Devenir intracellulaire des peptides et acides aminés
Pôle baso latéral de l’entérocyte vers le sang portal.
Absorption des lipides
Origine
60 à 150 g par jour de lipides constitués de triglycérides (80%) , de
phospholipides et de cholestérol.
Digestion intraluminale
1. Dans l’estomac, les triglycérides sont soumis à l’action de la lipase gastrique (active en milieu acide) et dégradé en diacylglycérol et acides gras.
2. Dans l’intestin, les triglycérides (micelles) sont soumis à l’action de la lipase pancréatique facilitée par la co-lipase, dégradés en monoacylglycérol et acides gras.
3. La digestion des phospholipides est uniquement intestinale après formation de micelles et action de la phospholipase A2 pancréatique
4. Les esters de cholestérol sont hydrolysés par la cholestérol estérase
pancréatique.
Absorption et transformation entérocytaire
Diffusion passive des acides gras et des monoacylglycérrols
Transport membranaire spécifique pour le cholestérol
Transformation en triglycérides et assemblage en lipoprotéines (chylomicrons et VLDL).
Absorption des vitamines
VITAMINES LIPOSOLUBLES
L’absorption des vitamines liposolubles est en relation très étroite avec celle des graisses et des esters de cholestérol.
VITAMINES HYDROSOLUBLES
1. Vitamine C absorbée par un symport NA+ - vit C
2. Vitamine B1 B2 B6 avec les protéines
3. Vitamine B12 : indispensable à l’érythropoïèse +++
- Source : protéines de la viande et du lait.
- Hydrolyse sous l’action de la pepsine et de l’acidité gastrique.
- Liaison au facteur R (haptocorrine) en milieu acide puis libération de la vitamine B12 grâce aux enzymes pancréatiques.
- En milieu neutre dans le duodénum : liaison au facteur intrinsèque (synthétisé par les cellules pariétales gastriques).
- Complexe FI – Vit B12 absorbé au niveau de l’iléon par un récepteur spécifique.
- Pathologie : déficit en F1 gastrite atrophie anémie de Biermer mal absorption iléale, pullulation bactérienne (consommation deB12), « grêle court)
Absorption du fer
Seule porte d’entrée : intestin.
Perte obligatoire de 1 mg/g donc besoin de 1 mg/j.
Sous forme de Fe+++ (ferrique) Fe++ (ferreux) plus soluble et en présence de vit C et acide et sous forme Fe – Hème dont absorption plus efficace.
L’absorption se fait au niveau du duodénum par 2 mécanismes différents :
1. récepteurs spécifiques pour Fe non lié à hème ; fixation à la ferritine (stockage) ; expression de récepteurs à la tranferrine sur la membrane basale qui favorisent la sortie du fer.
2. pour Fe –hème : traversée de la bordure en brosse ; action de l’hème oxygénase ; le fer se fixe à la ferritine.
Absorption du calcium
Les apports quotidiens varient entre 400 et 1000 mg.
HCl gastrique permet la solubilisation du calcium (CaCl2)
Dans l’intestin, l’acidité, la présence de sucre et d’acides aminés permettent le maintien du calcium en solution
Le calcium est absorbé par voie transcellulaire. La traversée de la bordure en brosse se fait par transport facilité dépendant de la concentration de Ca binding proteine intracellulaire et de l’extrusion active du Ca++ au pôle basal par une Ca++ ATPase et un échangeur Na+ - Ca++
Le mécanisme est saturable et vitamine D dépendant (1,25 diOH vit D3 régulant la synthèse de la CaBP). Il existe un mécanisme indépendant de la vitD.
Sécrétion pancréatique exocrine
1 – GENERALITES
2 – MORPHOLOGIE FONCTIONELLE
• acinus et lobules drainés par des canaux
• cellules zymogènes responsables de la sécrétion enzymatique
• cellules des canaux (cellules canalaires) responsables de la sécrétion hydro électrolytiques
• Zone commune pancréatique et biliaire commandée par un sphincter lisse unique : le sphincter d’Oddi
• Sécrètent l’insuline, le glucagon
3 – SUC PANCREATIQUE
Sécrétion hydro – électrolytique
Sécrétion des enzymes pancréatiques
- L’intestin est le siège principal de l’absorption des nutriments
- L’absorption est la résultante de flux permanents et abondants d’eau et de substances dissoutes de la lumière vers le milieu extracellulaire et vice-versa
- Le débit liquidien duodénal est de 10 L/jour avec une absorption nette de 9L/jour dans l’intestin grêle (1L/jour atteint le colon).
Anatomie fonctionnelle :
Duodénum : 30 cm de long, du pylore à l’angle de Treitz mélange avec les sécrétions pancréatique et biliaire
absorption passive par équilibration osmotique, rapide et peu régulée et intéresse surtout les glucides, l’eau et électrolytes.
Jéjunum : 3 à 4 m de long,absorption des glucides,des lipides et des protides,lieu de mouvements hydro-électrolytiques.
Iléon : 1 m de long ,absorption spécifique vit B12, sels biliaires.
Digestion et absorption des hydrates de carbones
Les glucides alimentaires : amidons et cellulose.
Les processus de digestion (hydrolyse) et d’absorption sont indissociables. La digestion des sucres débute dans la lumière intestinale sous l’action des alpha amylases salivaires et pancréatiques qui clivent les amidons en oligosaccharides et disaccharides. La cellulose est résistante aux amylases. Les dimères et oligosaccharides diffusent à travers le glycocalix
Action des disaccharidases de la bordure en brosse des entérocytes : (saccharase isomaltose +++) : hydrolyse en glucose et fructose.
Absorption et diffusion passive intercellulaire et intracellulaire.
La régulation fine de l’absorption des glucides se fait grâce à des protéines de transport dans la membrane plasmique.
Absorption des protéines
Origine
Exogène : 70 à 100 g par jour
Endogène : enzymes et glycoprotéines salivaires gastriques, pancréatiques et intestinaux (35g/j) et biliaires (10g/j).
Digestion intraluminale
Digestion incomplète par l’action des enzymes gastriques (pepsine) et pancréatiques (trypsine, chymotrypsine, peptidases) : production d’acides aminés et des peptides de taille variables.
Digestion entérocytaire
Au niveau de la bordure en brosse de l’entérocytes des peptidases.Clive en acides aminés et di-tri-peptides absorbés à travers la membrane.
Absorption intestinale des acides aminés
Au niveau de l’intestin proximal
Système de transport actif secondaire (gradient électrochimique de Na+)
Système de transport : diffusion facilitée.
Absorption intestinale des peptides
Pour les di et tripeptides : système spécifique co transport H+ - peptide
Le gradient H+ dépend de l’activité Na – K ATPase.
Devenir intracellulaire des peptides et acides aminés
Pôle baso latéral de l’entérocyte vers le sang portal.
Absorption des lipides
Origine
60 à 150 g par jour de lipides constitués de triglycérides (80%) , de
phospholipides et de cholestérol.
Digestion intraluminale
1. Dans l’estomac, les triglycérides sont soumis à l’action de la lipase gastrique (active en milieu acide) et dégradé en diacylglycérol et acides gras.
2. Dans l’intestin, les triglycérides (micelles) sont soumis à l’action de la lipase pancréatique facilitée par la co-lipase, dégradés en monoacylglycérol et acides gras.
3. La digestion des phospholipides est uniquement intestinale après formation de micelles et action de la phospholipase A2 pancréatique
4. Les esters de cholestérol sont hydrolysés par la cholestérol estérase
pancréatique.
Absorption et transformation entérocytaire
Diffusion passive des acides gras et des monoacylglycérrols
Transport membranaire spécifique pour le cholestérol
Transformation en triglycérides et assemblage en lipoprotéines (chylomicrons et VLDL).
Absorption des vitamines
VITAMINES LIPOSOLUBLES
L’absorption des vitamines liposolubles est en relation très étroite avec celle des graisses et des esters de cholestérol.
VITAMINES HYDROSOLUBLES
1. Vitamine C absorbée par un symport NA+ - vit C
2. Vitamine B1 B2 B6 avec les protéines
3. Vitamine B12 : indispensable à l’érythropoïèse +++
- Source : protéines de la viande et du lait.
- Hydrolyse sous l’action de la pepsine et de l’acidité gastrique.
- Liaison au facteur R (haptocorrine) en milieu acide puis libération de la vitamine B12 grâce aux enzymes pancréatiques.
- En milieu neutre dans le duodénum : liaison au facteur intrinsèque (synthétisé par les cellules pariétales gastriques).
- Complexe FI – Vit B12 absorbé au niveau de l’iléon par un récepteur spécifique.
- Pathologie : déficit en F1 gastrite atrophie anémie de Biermer mal absorption iléale, pullulation bactérienne (consommation deB12), « grêle court)
Absorption du fer
Seule porte d’entrée : intestin.
Perte obligatoire de 1 mg/g donc besoin de 1 mg/j.
Sous forme de Fe+++ (ferrique) Fe++ (ferreux) plus soluble et en présence de vit C et acide et sous forme Fe – Hème dont absorption plus efficace.
L’absorption se fait au niveau du duodénum par 2 mécanismes différents :
1. récepteurs spécifiques pour Fe non lié à hème ; fixation à la ferritine (stockage) ; expression de récepteurs à la tranferrine sur la membrane basale qui favorisent la sortie du fer.
2. pour Fe –hème : traversée de la bordure en brosse ; action de l’hème oxygénase ; le fer se fixe à la ferritine.
Absorption du calcium
Les apports quotidiens varient entre 400 et 1000 mg.
HCl gastrique permet la solubilisation du calcium (CaCl2)
Dans l’intestin, l’acidité, la présence de sucre et d’acides aminés permettent le maintien du calcium en solution
Le calcium est absorbé par voie transcellulaire. La traversée de la bordure en brosse se fait par transport facilité dépendant de la concentration de Ca binding proteine intracellulaire et de l’extrusion active du Ca++ au pôle basal par une Ca++ ATPase et un échangeur Na+ - Ca++
Le mécanisme est saturable et vitamine D dépendant (1,25 diOH vit D3 régulant la synthèse de la CaBP). Il existe un mécanisme indépendant de la vitD.
Sécrétion pancréatique exocrine
1 – GENERALITES
- Le pancréas est l’organe qui sécrète la plus grande quantité d’enzymes par rapport à sa masse
- Ces enzymes sont indispensables à la digestion
- Elles préparent les aliments pour permettre leur absorption optimale par l’épithélium de l’intestin grêle
2 – MORPHOLOGIE FONCTIONELLE
- Le pancréas exocrine :
• acinus et lobules drainés par des canaux
• cellules zymogènes responsables de la sécrétion enzymatique
• cellules des canaux (cellules canalaires) responsables de la sécrétion hydro électrolytiques
- Les canaux excréteurs
• Zone commune pancréatique et biliaire commandée par un sphincter lisse unique : le sphincter d’Oddi
- Le pancréas endocrine
• Sécrètent l’insuline, le glucagon
3 – SUC PANCREATIQUE
- Recueilli pur par cathétérisme rétrograde endoscopique du canal de Wirsung ou mélangé aux sécrétions duodénales et biliaires par tubage duodénal
- Liquide incolore, non visqueux, pH neutre à peu alcalin (7 à 8,4)
- Sécrétion de 1,5 à 2,5 L / jour
Sécrétion hydro – électrolytique
- Assurée par les cellules acineuses et surtout canalaires
- Les concentrations de Na et K sont indépendantes du débit sécrétoire, voisines du plasma
- La sécrétion des anions HCO3 et CL varie en fonction du débit sécrétoire
- La sécrétion de bicarbonates atteint 170 mM ; il s’agit d’une sécrétion active de bicarbonates par les cellules canalaires
- La sécrétion CL varie en sens inverse de celles des bicarbonates
Sécrétion des enzymes pancréatiques
- Le pancréas produit 6 à 20 grammes de protéines par jour
- Enzymes produites sous forme inactive ; ce sont des zymogènes
- L’activation est secondaire dans le duodénum grâce à une enzyme de la barrière en brosse des entérocytes : l’entérokinase
- L’entérokinase active le trypsinogène en trypsine
- C’est ensuite la trypsine qui va activer d’autres enzymes pancréatiques en chymotrypsine, colipase, élastase, carboxypeptidase, phospholipase
- La trypsine : 20 % de la sécrétion enzymatique
- Il s’agit d’une endopeptidase (agit au milieu des chaînes peptidiques) et reconnait comme substrats les acides aminés hydrophiles
- La chymotrypsine est une endopeptidase qui agit au niveau des acides aminés aromatiques
- Les carboxypeptidases sont des exopeptidases qui agissent sur les acides aminés de l’extrémité carboxy – terminales des chaînes peptidiques
 4 – REGULATION DE LA SECRETION PANCREATIQUE
4 – REGULATION DE LA SECRETION PANCREATIQUEA - Facteurs stimulants
La stimulation de la sécrétion pancréatique exocrine dépend surtout de
facteurs hormonaux
La sécrétine
- Libérée par les cellules endocrines S des cryptes duodénales
- Villosités apicales de la cellule S sensibles aux ions H +
- La sécrétine est libérée en réponse à l’acidité duodénale
- Responsable de la sécrétion HCO3 des cellules canalaires grâce à des récepteurs spécifiques (adénylyl cyclase - proteine G - AMP cyclique)
La cholécystokinine CCK
- Libérée par les cellules I duodénales et jéjunales
- Villosités apicales de la cellule I sensibles à la présence de lipides et de
- Stimule la sécrétion pancréatique exocrine des cellules acineuse
- Récepteurs spécifiques (proteine G - mobilisation de Ca++ intracellulaire – GMP cyclique)
Le nerf pneumogastrique X
- Effet stimulant sur la sécrétion pancréatique
- Faible importance
B - Facteurs inhibiteurs
- Effet de la somatostatine exogène
- Inhibiteur physiologique de la sécrétion pancréatique : inhibiteur de Cazal (trypsine)

PHYSIOLOGIE DU COLON
1 - Morphologie
Colon proximal : Cæcum, colon droit et moitié du colon transverse
Vascularisation : artère mésentérique supérieure
Rôle : absorption d’eau et électrolytes.
Colon distal : transverse, colon gauche, sigmoïde et rectum
Vascularisation : artère mésentérique inférieure
Rôle : stockage et évacuation des déchets de l’alimentation
2 - Absorption de l’eau et des électrolytes
- contrôle du volume et composition ionique des selles
- absorption de Na+ et Cl- et sécrétion de K+ et HCO3-
- conséquence : réabsorption d’eau avec concentration des matières fécales : 100mmol/L Na+ dans le cæcum à 10 mmol/L Na+ dans le rectum 1 Litre de débit liquidien dans le cæcum à 0,1 Litre dans le rectum
- Absorption de Na : Na K ATPase de la membrane baso latérale de la cellule colique régulée par l’aldostérone.
- Sécrétion de K+ : canaux potassiques.